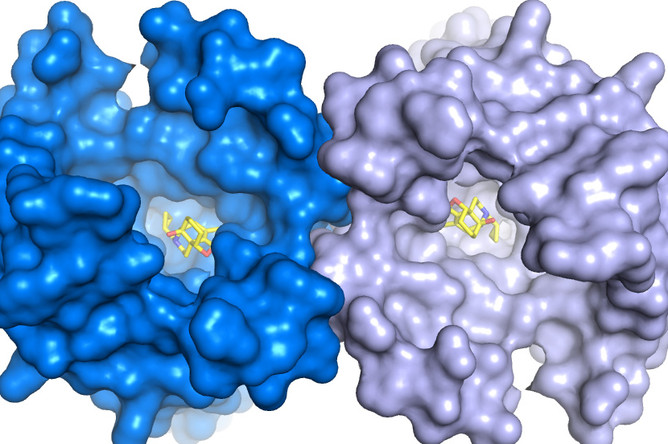
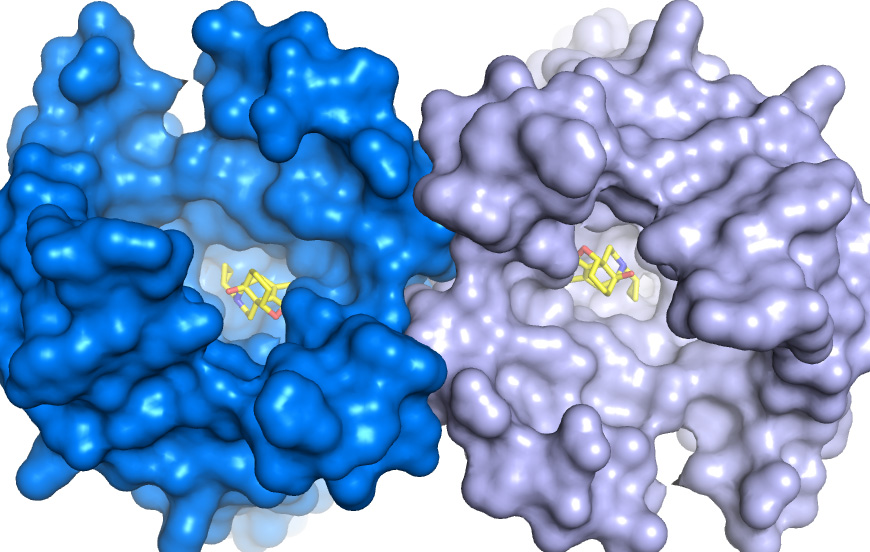
Впервые полностью определена трехмерная атомная структура двух человеческих опиоидных рецепторов — специфических молекул на контактирующей поверхности мембраны воспринимающей нервной клетки. Сразу две статьи с описанием этого открытия, которое можно рассматривать как существенный прорыв в понимании работы мозга и нервной системы, а также, потенциально, в индустрии анальгетиков, публикует сегодня Nature («Кристаллическая структура мю-опиоидного рецептора в связке с морфинным агонистом», и «Структура человеческого каппа-опиоидного рецептора в комплексе с JDTic»).
Опиоидные рецепторы — самые, наверное, широко известные нейромембранные молекулы, интерес к которым вызван ключевой ролью, которую они играют в формировании как болевых, так и приятных ощущений,
а также наркотической зависимости, депрессий, психозов, галлюцинаций и состояний измененного сознания.
В зависимости от того, с какими эндогенными (то есть производимыми самим организмом) белками-нейротрансмиттерами они связываются, различают четыре основные группы опиоидных рецепторов — μ- (мю), κ- (каппа), δ- (дельта) и ноцицептивные рецепторы. Первая греческая буква повторяет первую букву названия вещества (не обязательно эндогенного), с которыми впервые было обнаружено сродство рецептора, как, например, морфина в случае мю-рецептора или кетоциклазоцина в случае каппа-рецептора.
Детальную трехмерную структуру вплоть до пространственного расположения отдельных атомов пока удалось определить у двух из них — «мю» и «каппа».
Этим рецепторам грех жаловаться на отсутствие интереса к своей неоднозначной биохимической активности со стороны специалистов и широкой публики.
Так, мю-рецепторы отвечают за чувство удовольствия и ослабление болевых сигналов, охотно связываясь с такими нейротрансмиттерами, как эндорфины. Именно они являются главными мишенями популярных искусственно синтезированных опиоидов — морфина, героина, а также сильных анальгетиков мю-опиоидного ряда, например викодина — любимого лекарства доктора Хауса.
Каппа-рецепторы обрели славу относительно недавно в связи с широким распространением курительных смесей на основе шалфея предсказателей (Salvia divinorum) — растительного галлюциногена американских индейцев, действующее вещество которого — неоклеродановый дитерпеноид сальвинорин А — избирательно и эффективно связывается именно с ними.
skin: article/incut(default)
data:
{
"_essence": "test",
"incutNum": 3,
"pic2": "/files3/581/4100581/opioid_ill_v10.jpg",
"picsrc": "Художник помеcтил изображение опиоидного каппа-рецептора (спирали), связанного с агонистом группы морфинов, в цветок мака, хотя на невзрачном зеленом листике шалфея предсказателей в компании с молекулой сальвинорина А (высокоизбирательным активатором каппа-рецепторов) он смотрелся бы куда логичней. // Nature",
"repl": "<3>:{{incut3()}}",
"uid": "_uid_4100581_i_3"
}
отвечают за эффект, несколько отличный от действия мю-рецепторов, вызывая эмоциональную неуравновешенность, подавленность, панические атаки и очень яркие галлюцинации — как правило, недоброго характера.
Между тем, как показали эксперименты над животными, активация каппа-рецепторов также снимает болевой синдром, но с одним существенным отличием: в отличие от морфина, героина и анальгетиков мю-опиоидного ряда, агонисты (вещества, повышающие рецепторный отклик) каппа-рецепторов не вызывают привыкания. Поэтому, если удастся модифицировать их формулу так, чтобы свелся к минимуму непредсказуемый психотический эффект,
медики получат в распоряжение сильные болеутоляющие лекарства нового поколения без «наркотической ауры», с которой никак не хотят расставаться мю-опиоидные агонисты.
«Теперь, зная строение каппа-рецептора и точную форму его молекулы, фармацевты могут существенно ускорить работу», — считает Брайан Рот, биохимик из Университета Северной Каролины, участвовавший в расшифровке рецептора, один из авторов статьи в Nature.
Мощный психоделический эффект каппа-активации тоже не стоит игнорировать при изучении механизмов восприятия, сознания и конструирования мозгом картины мира.
«По всей видимости, каппа-рецепторы играют очень важную роль в нашем восприятии реальности»,
— подчеркнул Рот в одном из пресс-релизов публикации. После нескольких десятилетий запретов на научное изучение психоделиков работы в этой области, наконец, активизировались, и об одном из таких исследований мы уже писали.
Работа по расшифровке каппа-рецептора велась в несколько стадий.
Сначала была решена нетривиальная задача по выделению и сохранению нестабильной молекулы рецептора, выделенной из культуры нервных клеток гусениц генномодифицированной моли (Spodoptera frugiperda), несущих ген, отвечающий за экспрессию каппа-рецепторного белка человеческого типа. Сделать это удалось, надежно стабилизировав нужный белок с помощью молекулы-антагониста — экспериментального лекарства JDTic (одного из производных 4-фенилпиперидина), избирательно блокирующего каппа-рецептор.
skin: article/incut(default)
data:
{
"_essence": "test",
"incutNum": 5,
"pic2": "/files3/581/4100581/What-is-Salvia.jpg",
"picsrc": "Шалфей предсказателей -- неприхотливое растение, легко выращиваемое в комнатных условиях. Его листья содержат разные модификации сальвинорина (A, B и С) -- сильного избирательного агониста опиоидных каппа-рецепторов, научное изучение которого только начинается. Сальвинорин, как и антагонист каппа-рецепторов - экспериментальный анальгетик JDTic, могут послужить основой для синтеза болеутоляющих неморфиноподобных средств нового поколения // Wikimedia",
"repl": "<5>:{{incut5()}}",
"uid": "_uid_4100581_i_5"
}
исследователи получили точную трехмерную модель каппа-рецептора с разрешением 2,9 ангстрем.
По той же схеме, только с участием генномодифицированных мышей и другой разновидности антагониста-ловушки, была получена трехмерная модель мю-рецептора, которая поможет понять, как именно стыкуются с его молекулой различные опиоидные лиганды, не дающие спокойно спать сотрудникам служб наркоконтроля. Что, в свою очередь, также поможет очистить от побочных эффектов действие опиоидных лекарств, воздействующих на мю-рецепторы.